ソフトカプセル(軟カプセル)技術を活用した難水溶性薬物への対応
難水溶性薬物の経口製剤開発:課題と技術的対応
医薬品開発において、難水溶性薬物の開発候補品は増加しています。難水溶性化合物は、医薬品開発の妨げとなる可能性もあり、製剤技術の課題として対応が必要です。特に経口投与を前提とした製剤では、溶解性の低さは吸収性(バイオアベイラビリティ:BA)に直結するため、製剤設計の初期段階から溶解性改善策を講じることが不可欠です。
本コンテンツでは、難水溶性薬物を対象とした医薬品開発における製剤技術での対処とソフトカプセルの有用性を紹介し、グリーンカプス製薬での取り組みを説明します。
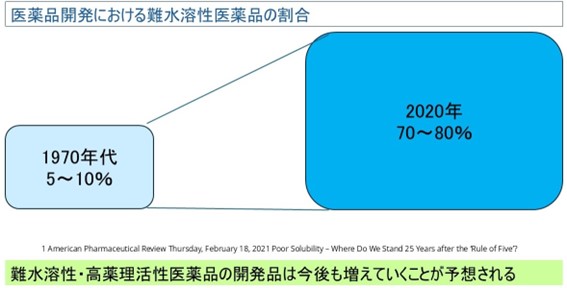
医薬品開発における難水溶性薬物の増加
難水溶性の新薬候補はこの数十年で飛躍的に増加し、1970年代にはわずか5~10%であった難水溶性化合物の割合が、2020年には全体の約70~80%と推測されていることが報告されています。1
難水溶性薬物について、かつては初期スクリーニングで淘汰される傾向にありましたが、現在では、製剤技術で克服する前提に開発が進められるようになっています。1
そのため、難水溶性候補化合物への製剤設計での対応の、医薬品開発における重要性は高まってきています。
難水溶性薬物の医薬品開発(製剤開発)における課題
初期臨床試験における課題
医薬品開発の初期段階では、特に候補薬物の評価を早く実施する必要性があります。有効成分の溶解性または透過性が低く、体内吸収少ない場合、初期の臨床試験(フェーズI)において、適正な安全性・有効性に関する評価結果が得られないことが考えられます。そのため、初期開発の段階から製剤技術によって溶出性を改善した試験製剤を用いる必要性が生じます。2
CMC(Chemistry, Manufacturing and Controls)上の課題
難水溶性薬物の製剤設計は、ソフトカプセルを除いて特殊な技術を要することもあります。開発が後期(フェーズⅡ・Ⅲ)において製剤設計方針や剤形を変更する場合は、製造・品質管理(CMC)上の課題が発生するため、開発後期の方針変更は最小限に抑えるのが望ましいです。
製剤変更に伴う課題:
- 生物学的同等性の確認:変更前後の製剤でのバイオアベイラビリティが同等であることを示すため、ヒトによる生物学的同等性試験や溶出比較試験が求められる。
- 開発スケジュールへの影響:製剤変更に伴う品質試験の追加や安定性試験データの実施により開発期間・コストが増加する可能性がある。
- 製剤間の性能差:初期製剤で得られた有効性・安全性が、ブリッジング製剤でも再現する必要がある
よって、難水溶性薬物の医薬品開発においては、初期開発における早急性と開発途中におけるリスクとコストを鑑みて、初期臨床の段階から市販製剤を見据えた一貫した製剤コンセプトで進めるか、開発途中で製剤を市販に最適なものに切り替えるかの決断も必要です。ソフトカプセル技術であれば、初期開発から一貫した製剤コンセプトでの開発が可能です。
難水溶性薬物に対する製剤技術の対応
上述の通り、難水溶性の薬物では適切な製剤設計と方針を定め、開発を進める必要があります。経口製剤の剤形として代表的な「錠剤・硬カプセル(固形製剤)」「内用液剤(経口液剤)」「ソフトカプセル(軟カプセル)」の3種類について、それぞれ難水溶性薬物への対応策と特徴を比較します。
表.難水溶性薬物に対する製剤技術での対応(剤型別)
|
剤型 |
主な対応方法 |
メリット |
デメリット |
|
ソフト |
・油性溶媒を使用 |
・難水溶性薬物でも容易に |
・製造工程が特殊で専用 ・内容液と皮膜との相互作 |
|
錠剤・ |
・微粒子化(ナノ粒子化等) ・固体分散体 薬物を水溶性担体(例:ポ |
・多くの難水溶性薬物に |
・製剤技術の難易度が高 ・非晶質化の場合、経時的 ・高用量薬物では溶出量の |
|
内用液剤 |
・pH調整 |
・投与時点で薬物が溶解 ・難水溶性薬物でも液状に |
・保存中の安定性に注意が ・臨床試験実施時の手間が ・消化管内で希釈されると |
ソフトカプセルでのバイオアベイラビリティの改善
ソフトカプセルは、難水溶性薬物のバイオアベイラビリティを向上します。ソフトカプセルと錠剤の比較では、ジゴキシンやサキナビルでは、Cmax・AUCが有意に高く、イブプロフェンでは速やかな効果発現が確認されました。シクロスポリンでは、自己乳化製剤技術により、個体差や食事の影響が軽減された報告もあります。これらの結果は、ソフトカプセルがバイオアベイラビリティの課題を解決し、治療効果と患者利便性の両立を可能にすることを示しています
表.ソフトカプセルの医薬品の吸収性
|
薬物(BCS分類) |
比較剤型 |
吸収・生体利用率の結果 |
|
ジゴキシン(BCS IV or II) |
ソフトカプセル vs 錠剤 |
Cmax:有意に高い |
|
イブプロフェン(BCS II) |
ソフトカプセル vs 糖衣錠 vs 速崩壊錠 |
Cmax: 糖衣錠・速崩壊錠より有意に高い |
|
サキナビル(BCS IV) |
ソフトカプセル vs 硬カプセル |
Cmax, AUC: 有意に高い |
|
シクロスポリン(BCS IV) |
Neoral®(自己乳化) vs Sandimmune®(油性) |
Cmax, AUC, Tmax: 個体間・個体内バラツキ改善、食事の影響減少 |
- Catenazzo et al. (1977)
“Bioavailability of Digoxin in a New Soluble Pharmaceutical Formulation in Capsules”
Journal of Pharmaceutical Sciences, 66(2), 267–269 - Schettler T et al. (2001)
“Comparative Pharmacokinetics of Two Fast-Dissolving Oral Ibuprofen Formulations and a Regular-Release Ibuprofen Tablet”
Clinical Drug Investigation, 21(1): 73–78 - ADIS Drug Evaluation (2000)
Saquinavir Soft-Gel Capsule: An Updated Review of its Use in the Management of HIV Infection AUG 60(2), 481–516 - Cyclosporin A Review
A pharmacokinetic and clinical review of the potential clinical impact of using different formulations of cyclosporin A
総括(おわりに)
難水溶性薬物の医薬品開発は、今後も、必要性が高まることが予想されます。
ソフトカプセルは、難水溶性薬物の製剤化において、容易に有効成分を溶解することで、有効成分のバイオアベイラビリティを担保し、開発スピードに貢献します。さらに、自己乳化技術を活用することで、更なるバイオアベイラビリティの改善や体内でのばらつき低減が期待できる有力な選択肢です。3製剤開発初期から市販製剤に近い製剤設計が可能な点は開発効率やリスク管理の面での利点にのみでなく、開発期間を短縮によるスピーディーな市場投入を実現します。
ソフトカプセル製剤は、難水溶性薬物の課題に対する実用的かつ戦略的な解決策として、有効な手段の一つです。
グリーンカプス製薬では、製剤処方検討に対するデータの体系的な活用等により、ソフトカプセルの利点を活かした提案をします。また、ハード面では高薬理活性医薬品対応のR&D及び生産機器を有しており、医療現場のニーズや開発状況に合わせて、一貫した対応が可能です。
参考文献一覧:
- Moreton, C. (2021). “Poor Solubility – Where Do We Stand 25 Years after the ‘Rule of Five’?” American Pharmaceutical Review, Feb 18, 2021.
- Alex Del Priore(2025).Formulating OSDs for Poorly Soluble Drugs
- 3.自己乳化製剤の原理と技術概要(https://www.greencaps.co.jp/develop-manufacture/develop/self-microemulsifying/)
